Por Dr. Julival Ribeiro – HBDF / Revisão: Dra. Nancy Bellei – DIP/UNIFESP
O médico infectologista com especialização nos EUA e ex-diretor geral do Hospital de Base do DF (HBDF), Dr. Julival Ribeiro, traz um estudo detalhado do vírus influenza, e vários esclarecimentos a população, através de um questionário de perguntas e respostas, para dirimir dúvidas.
Segundo a OMS, as epidemias anuais, resulta em 1 bilhão de casos de Influenza no mundo, resultando em torno de 3 a 5 milhões de casos graves e aproximadamente 250.000 a 500.000 mortes.
Dados de Influenza no Brasil, no ano de 2017 – registrados pelo Sistema de Informação da Vigilância Epidemiológica da Gripe (SIVEP-GRIPE), do Ministério da Saúde – apontam para o crescimento da incidência do subtipo H3N2 do vírus da Influenza A. Até a décima semana epidemiológica, que se estendeu de 01 de janeiro a 11 de março de 2017, houve predomínio do subtipo da Influenza A (H3N2) em mais de 60% das amostras analisadas.
Nos últimos anos, o vírus H3N2 vem sofrendo alterações antigênicas importantes, durante uma mesma temporada de gripe, o que determina revisões dos componentes vacinais anuais; desta forma, eventualmente, inclusive indivíduos vacinados podem apresentar síndromes gripais e complicações relacionadas à infecção por AH3N2.
Alguns estudos incluindo pacientes hospitalizados – infectados com Influenza A H1N1pdm09 ou A (H3N2) – mostraram maior taxa de complicações e óbito por H3N2 em indivíduos de faixa etária mais elevada (>49 anos), comparados à população mais jovem; além disso, as alterações laboratoriais – como a carga viral, alterações da PCR (proteína c reativa) e leucocitose ou leucopenia – são mais relevantes.
A associação com a pneumonia bacteriana e a apresentação de pneumonia lobar após 5 dias da doença costumam também ser mais frequentes, particularmente nos indivíduos mais velhos, com comorbidades respiratórias e cardiovasculares. Classicamente, a mortalidade por H3N2 é elevada dentre pacientes idosos, seja pela pneumonia, seja por complicações da doença de base.
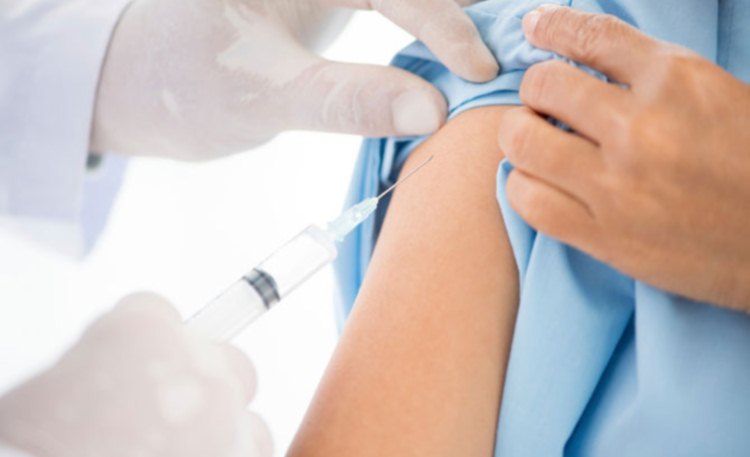
A vacina é a melhor estratégia disponível para a prevenção da gripe e suas consequências, proporcionando impacto indireto na diminuição do absenteísmo no trabalho e dos gastos com medicamentos para tratamento de infecções secundárias, das internações hospitalares e da mortalidade evitável.
Todo ano, no Brasil, ocorre uma epidemia de gripe sazonal, geralmente entre abril e outubro, sobretudo nos estados onde as condições climáticas são mais definidas. Vale lembrar, que a umidade relativa do ar (quantidade de vapor de água na atmosfera) desempenha um papel importante na transmissão do vírus da Influenza (menor umidade relativa e clima mais seco, maior transmissão do vírus).
Segundo o CDC/EUA, não é possível prever o comportamento da gripe a cada ano no que tange ao momento em que ela se dissemina, em relação à gravidade e a duração da estação, que pode variar de um ano para o outro, mesmo dentro de regiões de um mesmo país. O impacto das epidemias de Influenza é reflexo da interação entre a variação antigênica viral, o nível de proteção da população para as cepas circulantes e o grau de virulência dos vírus.
INFLUENZA (GRIPE)
Há 3 tipos de vírus da Influenza, chamados de Influenza A Influenza B e Influenza C já detectados na espécie humana. O vírus da Influenza D foi detectado no gado e em suínos. Influenza A e B estão associados com a Influenza sazonal e com muitos surtos e epidemias. Influenza C é relativamente rara e usualmente não causa surtos ou epidemias. A Influenza A pode infectar humanos, bem como pássaros, porcos e outros animais. Influenza B e C são patógenos humanos. Em relação ao vírus da Influenza D não se sabe infecta ou causa doenças nas pessoas.
Leia também: H1N1: Mitos, verdades e esclarecimentos
A classificação em subtipos da Influenza tipo A é baseada nas características de duas glicoproteínas da cápsula viral: Hemaglutinina (HA) e a Neuraminidase (NA). Atualmente, são conhecidos 18 subtipos de HA e 11 subtipos de NA. Historicamente, três subtipos de HA (H1, H2 e H3) adquiriram a habilidade de serem transmitidos eficientemente entre humanos. Entretanto, outros subtipos, como H5, H6, H7 e H9, ocasionalmente, acometem humanos e são considerados possíveis ameaças para uma futura pandemia. A combinação entre a HA e NA é que dá o nome do subtipo (H1N1, H1N2 e assim sucessivamente). A influenza do tipo B é dividido em duas linhagens: Victoria e Yamagata.
Os vírus da Influenza são os únicos entre os vírus respiratórios com imensa capacidade de mutação, criando novos vírus com material genético diferente do que lhe deu a origem.
Pequenas mutações antigênicas (drift) geram novos sorotipos (cepas) em relação a uma temporada sazonal para a outra e pode resultar em epidemia devido a essa nova cepa. Essas pequenas mutações ocorrem em ciclos aproximadamente anuais. Por isso, as epidemias de gripe ocorrem anualmente e se faz necessário uma nova composição da vacinação anual, pois os anticorpos formados contra as cepas anteriores podem não responder adequadamente contra as cepas novas do vírus.
Em relação às mutações antigênicas maiores (shift) há trocas de moléculas na Hemaglutinina (HA) e a Neuraminidase (NA) e ocorre somente com o vírus Influenza A. Esse fenômeno ocorre em menor frequência e, em aproximadamente, 40 anos. Quando ocorre esse novo subtipo, a chance de uma pandemia é grande, em virtude de não termos ainda imunidade.
Em 2009, um novo vírus da Influenza A (novo subtipo H1N1), originado no México, se espalhou rapidamente pelo mundo. Ficou conhecido o vírus Influenza pandêmico H1N1 2009.
Perguntas e respostas sobre a Influenza H1N1
- Que é Influenza?
Resposta: Influenza ou gripe é uma infecção viral aguda do trato respiratório, comunitária, com distribuição global e elevada transmissibilidade.
- Quais os vírus que causam Influenza?
Resposta: O agente etiológico da gripe é o Myxovirus influenzae, também denominado vírus Influenza.
- Quais os Reservatórios da dos vírus Influenza A B e C?
Resposta: Os vírus da Influenza A estão presentes na natureza em diversas espécies, incluindo humanos, aves, suínos, cavalos, focas e baleias. Os vírus Influenza B e C têm como reservatório somente seres humanos.
- Como ocorre a transmissão?
Resposta: A transmissão ocorre por contato direto (pessoa-pessoa) ou através de superfícies ou objetos contaminados (indireta). A transmissão direta ocorre através de gotículas de aerossol (> 5 micras de diâmetro) expelidas durante o ato de espirrar, tossir ou falar de indivíduo infectado. A pessoa com Influenza pode transmitir o vírus a outras pessoas até aproximadamente a 1 metro e meio de distância. Essa disseminação ocorre mais facilmente em ambientes fechados, sobretudo no inverno, quando as pessoas ficam por mais tempo juntas.
Transmissão indireta – uma pessoa pode adquirir Influenza ao tocar com as mãos, uma superfície ou um objeto contaminado com o vírus da Influenza e em seguida tocar os olhos, boca ou nariz. Estudos têm demonstrado que o vírus da Influenza pode sobreviver por 24 a 48 horas em superfícies como mesas de cafeterias, livros, superfícies rígidas, teclado de computador, maçanetas e mesas de escritório. Lavar as mãos com frequência ajuda você a reduzir as chances de se contaminar a partir desses objetos e superfícies.
- Quais as medidas para reduzir a transmissão da Influenza?
Resposta: Vacinar anualmente.
– Boas práticas de Higiene: Higienização das mãos com água e sabão ou usar álcool-gel a 70%.
– Evitar manipular lenços ou objetos usados por uma pessoa doente.
– Utilizar lenço descartável ao espirrar, tossir ou falar e jogar o lenço no lixo após o uso.
– Pessoas doentes devem permanecer em casa, evitando ir ao trabalho ou à escola.
Se não tiver lenços de papel, use o cotovelo ao tossir ou espirrar e, em seguida, lave as mãos.
Caso seja necessário ir a uma Unidade de Saúde, comunique que está gripado e solicite uma máscara cirúrgica para evitar a transmissão para outras pessoas.
- Qual o período de incubação da Influenza?
Resposta: 1 a 4 dias. Um único indivíduo infectado pode transmitir a doença para um grande número de pessoas suscetíveis.
- Qual o período de transmissibilidade?
Resposta: 1 dia antes do início dos sintomas e até 7 dias após o início dos sintomas; entretanto, os indivíduos afebris há mais de 24 horas não apresentam mais um risco importante de transmissão na comunidade. Esse período depende da idade e de doenças que a pessoa possua. Em crianças e em pacientes imunossuprimidos, esse período pode ser mais prolongado.

- Qual a diferença entre síndrome gripal e Síndrome Respiratória Aguda Grave?
Resposta: Síndrome gripal: Na ausência de outro diagnóstico específico, considerar o paciente com febre, de início súbito, mesmo ainda que referida, acompanhada de tosse ou dor de garganta e pelo menos um dos sintomas: mialgia, cefaleia ou artralgia.
SRAG – indivíduo de qualquer idade, com internação hospitalar, por doença respiratória aguda grave caracterizada por febre, tosse e dispneia, acompanhada ou não dos seguintes sintomas: aumento da frequência respiratória de acordo com a idade, hipotensão em relação à pressão arterial habitual do paciente; em crianças, além dos itens acima, observar também: batimentos de asa de nariz, cianose, tiragem intercostal, desidratação e inapetência.
A dificuldade para respirar pode ser um sinal importante para a doença, assim como a presença de hipoxemia, desidratação, sonolência e a persistência da febre por mais de 72h.
- Há alguma diferença entre gripe sazonal (gripe comum) e a gripe causada pelo H1N1?
Resposta: Não. Os quadros clínicos são os mesmos. Entretanto, a infecção grave com a necessidade de internação ou com complicações fatais é significantemente maior nas infecções causadas pela Influenza A (H1N1) que nas causadas pela Influenza B.
As situações reconhecidamente de risco para o desenvolvimento de formas graves e de óbito da Influenza gripe H1N1 são: gestação, idade menor do que 2 anos ou maior que 60 anos e presença de comorbidades, como doença pulmonar crônica, cardiopatias (insuficiência cardíaca crônica), doença metabólica crônica (obesidade mórbida, diabetes), imunodeficiências, insuficiência renal crônica, entre outras.
- Quais as complicações mais frequentes da Influenza?
Resposta: Pneumonias bacterianas secundárias, pneumonia viral primária, miosite, miocardite, pericardite, síndrome de Guillain-Barré, encefalite e mielite transversa.
- Como fazer o diagnóstico laboratorial?
Resposta: De forma geral, a amostra preferencial para o diagnóstico laboratorial é a secreção da nasofaringe, colhido de preferência nos primeiros três dias do aparecimento dos sinais e sintomas. Seguir a técnica recomendada pelo Laboratório.
12 – Como é feito o tratamento?
Resposta: O antiviral Oseltamivir quando indicado deve ser utilizado preferencialmente nas primeiras 48 horas pois quanto mais precoce maior a eficácia. Em pacientes hospitalizados os estudos mostraram algum benefício na redução da mortalidade em pacientes que iniciaram o tratamento até 96 horas. Portanto, iniciar o tratamento mesmo sem o resultado do exame para detectar vírus da Influenza. Atentar para as interações medicamentosas, as contraindicações e os efeitos colaterais.
- Quem deve tomar a vacina?
Todas as pessoas deveriam se vacinar, exceto crianças abaixo 06 meses. Não existe nenhuma contraindicação a pessoas saudáveis, fora do grupo de risco, fazer uso da vacina. Todas as crianças abaixo de nove anos de idade, que estejam tomando a vacina para Influenza pela primeira vez, devem receber duas doses com um mês de intervalo.
Foto: reprodução internet
Quem é considerado grupo de risco para receber a vacinação oferecida pelos Serviços Público de Saúde?
Resposta: Crianças de 6 meses a 5 anos, gestantes, puérperas, trabalhador de saúde, povos indígenas, indivíduos com 60 anos ou mais de idade, adolescentes e jovens de 12 a 21 anos sob medidas socioeducativas, população privada de liberdade, funcionários do sistema prisional, pessoas portadoras de doenças crônicas, pacientes imunossuprimidos ou que estejam fazendo uso de medicações imunodepressoras. Crianças e adolescentes dos 6 meses aos 18 anos que estejam recebendo terapia prolongada com aspirina e, portanto, estejam sob risco de desenvolver Síndrome de Reye, após adquirir a Influenza. Neste ano o Ministério da Saúde ampliara a vacinação para os professores.
- Por que se deve tomar a vacina da Influenza anualmente?
O vírus Influenza induz altas taxas de mutação durante a fase de replicação, em especial, da hemaglutinina e neuraminidase, as duas glicoproteínas de superfície do vírus. Estas mutações ocorrem de forma independente e provocam, habitualmente, o aparecimento de novas variantes para as quais a população ainda não apresenta imunidade, já que a infecção prévia por determinada cepa confere pouca ou nenhuma proteção contra os vírus de surgimento mais recente. O efeito da vacina garante apenas um período de 6 a 10 meses de imunização, fazendo-se necessária a vacinação anualmente.
A rede de vigilância epidemiológica da gripe coordenada pela Organização Mundial de Saúde (OMS) é realizada em vários países. As cepas de vírus Influenza coletadas nos vários países, inclusive no Brasil, são classificadas e catalogadas de acordo com os critérios estabelecidos pela OMS. Após essa análise, se determina a composição das cepas do vírus Influenza A e B a serem incluídas na composição da vacina que será disponibilizada no ano seguinte.
Por exemplo: a cepa A/Sydney/5/97 (H3N2) é uma variante do tipo A, de origem humana, isolada na cidade de Sydney em 1997, com antígenos de superfície H3 e N2.
O H1N1 não apresentou mutação relevante do ponto de vista antigênico desde 2010, o que fez com que a vacina continuasse sendo eficaz contra a Influenza A causada pelo subtipo H1N1. Entretanto, pela primeira vez desde 2010, a vacina trará uma nova cepa do vírus Influenza A/H1N1 para o ano de 2017, isso porque foi constatado que o vírus sofreu alterações genéticas no último ano. De 2016 para 2017, a única mudança da composição da vacina contra gripe será a cepa do vírus Influenza A (H1N1), os demais permanecerão iguais, pois não ocorreram mutações nessas linhagens.
- Qual a composição da vacina para o ano de 2017?
Resposta: As vacinas contra a influenza a serem utilizadas no Brasil em 2017 terão nova composição. Em acordo com determinação da Organização Mundial da Saúde (OMS) em relação à situação das cepas da gripe em circulação no mundo, a Anvisa/ M.S. publicou a orientação para composição do produto no próximo ano. A medida está na RDC 119/2016 publicada no último mês de outubro. Pela primeira vez desde 2010, a vacina trará uma nova cepa do vírus Influenza A/H1N1. Isso porque foi constatado que o vírus sofreu alterações genéticas no último ano.
São três tipos de cepas de vírus em combinação:
– um vírus similar ao vírus influenza A/Michigan/45/2015 (H1N1) pdm09;
– um vírus similar ao vírus influenza A/Hong Kong/4801/2014 (H3N2);
– um vírus similar ao vírus influenza B/Brisbane/60/2008 (Victoria).
As vacinas influenza chamadas quadrivalente, contendo dois tipos de cepas do vírus influenza B, deverão apresentar um vírus similar ao Influenza B/Phuket/3073/2013 (Yamagata), adicionalmente aos três tipos de cepas especificadas pela resolução RDC.
- Quais as vacinas para Influenza estão disponíveis no Brasil? Quais as diferenças entre elas?
Existem dois tipos de vacina: a trivalente e a quadrivalente. Uma dose de vacina trivalente cobre os dois subtipos do vírus influenza A — o H1N1 Michigan e o H3N2 Hong Kong — e um subtipo da influenza B, o Brisbane. A vacina tetravalente oferece ainda proteção para um segundo subtipo da influenza B, o Phuket. Ambas imunizam o H1N1 (vírus influenza do tipo A).
- Quanto tempo após tomar a vacina começa a produção de anticorpos?
Resposta: Após duas a três semanas da vacinação começa a produção de anticorpos contra a Influenza. É recomendável que a vacinação seja realizada anualmente nos meses de outono, objetivando-se, assim, que os níveis máximos de anticorpos sejam coincidentes com os meses de inverno, onde a doença é mais incidente em consequência da maior circulação vírus.
- O grau de proteção após a imunização é igual para todas as pessoas?
Resposta: A eficácia da vacina é de 50-85%. A resposta na produção de anticorpos após a vacinação depende de vários fatores, incluindo a idade, exposição prévia e subsequente aos antígenos e a presença de condições que alteram a resposta imunológica. Se você tem sido vacinado contra Influenza e por um acaso adquirir uma Gripe, ela será menos grave, sendo menos provável de desenvolver complicações.
- Há risco de uma pessoa tomar vacina da Influenza e adquirir Gripe?
Resposta: Não. A vacina é composta apenas por vírus inativado.
- Quais os efeitos colaterais da vacina para Influenza?
Resposta: Aplicada por injeção, a vacina pode causar desconforto no local da aplicação e um mal-estar leve e passageiro (no máximo 24 horas após a aplicação), como se fosse o início de um resfriado.
- Qual o risco de pessoas com doenças crônicas não transmissíveis apresentar reações à vacina?
Resposta: A possibilidade de ocorrer um evento adverso após a vacinação em pessoas com doença crônica é semelhante a qualquer outro indivíduo.
- Quais os componentes das vacinas usadas no ano de 2017?
Os componentes da vacina Fluzone (Sanofi) são: Octilpenol etoxilato e formaldeído. Na apresentação de dose única da vacina não há preservativo. Na de múltiplas doses há o (thimerosal-mercúrio). Não contém adjuvante.
Os componentes da vacina Fluarix Quadrivalente (GSK) é formulada sem preservativos. Cada dose contém octoxinol (TRITON® X-100), α-tocoferol e polisorbatol (Tween 80). Cada dose, também, pode conter quantidades residuais de: hidrocortisona, gentamicina, ovoalbumina, formaldeído e deoxicolato usadas no processo de fabricação. Não contém adjuvante.
A vacina fabricada pelo Instituto Butantan – é uma vacina trivalente e cada dose de 0,5 ml contém: formaldeído, traços de neomicina e triton X-100 (octoxinol9). Não contém adjuvante.
Na produção da vacina, os vírus da vacina são propagados em ovos embrionados de galinha.
- Há novas recomendações em relação à vacinação para Influenza em pessoas com alergia a proteína do ovo?
Resposta: Sim. Baseado nas novas recomendações do Centro Controle de Doenças (CDC) /EUA e do Comitê Consultivo sobre Práticas de Imunização ((ACIP) / EUA, 2016 / 2017, pessoas com alergia a proteína do ovo podem receber a vacina da Influenza.
Novas recomendações segundo o CDC/EUA:
– Pessoas com história de alergia a proteína do ovo (ovoalbumina) que apresentarem apenas urticária podem receber a vacina contra gripe.
– Pessoas com história de reação alérgica grave a proteína do ovo, isto é, qualquer outro sintoma diferente de urticária, tais como (angioedema, desconforto respiratório, tontura, ou vômitos recorrentes; ou que necessitaram de adrenalina ou outra intervenção médica de emergência, pode receber a vacina da gripe, desde que seja administrada no Hospital e sobre supervisão médica).
Pessoas com alergia a proteína do ovo não necessita ficar em observação por 30 minutos após receber a vacina para influenza como era recomendado anteriormente. Para qualquer tipo de vacina injetável, Incluindo a da gripe, pode ocorrer síncope; desta forma se recomenda a pessoa ficar em observação por 15 minutos.
Reação alérgica grave, após vacinação contra a gripe, independentemente do componente suspeito de ser responsável pela reação, é uma contraindicação para receber futura vacina para gripe.
Considerações:
– A alergia ao ovo afeta aproximadamente 1,3% de todas as crianças e 0,2% de todos os adultos.
– Se uma pessoa é capaz de comer ovo levemente cozido (por exemplo, ovo mexido) sem reação, é improvável que você seja alérgico e pode receber qualquer vacina contra a gripe.
– A maioria das vacinas contra a gripe, no seu processo de fabricação usa-se ovos e contêm desta forma uma pequena quantidade de ovoalbumina.
– Embora nem todos os fabricantes revelem a quantidade de ovoalbumina nas suas vacinas, os que fizeram a partir de 2011-12 até 2014-15 relataram quantidades máximas de dose de ≤1 μg / 0,5 mL para vacinas contra a gripe. A vacina contra a gripe de base celular (Flucelvax) é preparada a partir de vírus propagados em células de rim canino e contêm pequena quantidade de ovoalbumina (5 × 10-14 mcg/0.5 mL).
– A vacina recombinante (Flublok) é a única vacina atualmente disponível que está completamente livre de ovoalbumina.
Diversos estudos publicados têm relatado que o risco de anafilaxia associada com vacina para influenza em pacientes alérgicos a proteína do ovo é muito baixo.
Em 2012, foi realizado uma revisão dos estudos publicados, inclui 4172 pacientes alérgicos ao ovo (dos quais 513 relataram história de reação alérgica grave) e não relataram casos de anafilaxia após a administração da vacina inativada contra influenza. O maior estudo na revisão incluiu 830 pessoas alérgicas (dos quais 164 relataram história de reação alérgica grave ao ovo) e apenas 17 (2%) desses pacientes apresentaram qualquer evento adverso. Todos os eventos adversos foram leves; Eles incluíram dor abdominal, urticária e sintomas respiratórios, como dispneia.
Segundo dados do CDC/EUA – ocorreram 10 casos de anafilaxia após serem administradas 7.4 milhões de doses de vacina inativada contra a gripe (taxa de 1,35 por um milhão de doses). A maioria destes casos de anafilaxia não estava relacionada com a proteína do ovo presente na vacina.
- Existe alguma vacina fora do Brasil que não contém na sua composição a proteína do ovo?
Resposta: Sim. Ela é aprovada para uso em adultos maiores de 18 anos. Essa vacina é fabricada usando a tecnologia recombinante, não usando no processo de fabricação nem vírus da influenza nem ovos. É uma vacina trivalente.
- Eu posso pegar a gripe ingerindo ou preparando carne de porco?
Resposta: Não. O vírus da Influenza não se transmite pela comida.
- A vacina da Influenza pode interferir no resultado de alguns exames laboratoriais?
Resposta: Sim. A vacina Influenza (fragmentada e inativada) pode interferir na resposta a alguns testes laboratoriais para vírus, como HIV-1, vírus da hepatite C e HTLV-1.
- Deve as gestantes receber a vacina trivalente ou quadrivalente inativada para Influenza?
Resposta: Sim. Em qualquer período da gestação.
As gestantes têm risco aumentado de complicações, devido a alterações que ocorrem naturalmente no sistema imune durante a gestação. A própria gravidez pode levar a certa dificuldade na respiração, isso é, particularmente, relevante no segundo e terceiro trimestre da gestação.
Há recomendação que todas gestantes, em qualquer período da gravidez, receba a vacinação contra a Influenza, devido ao risco de graves complicações associadas ao aumento de hospitalização e óbito em gestantes expostas ao vírus. Há evidência que a vacinação em gestantes protege os recém-natos de adquirir Influenza por até 6 meses, menos probabilidade de prematuridade, aborto e de recém-nato com baixo peso ao nascer. Estudos de vacinação da Influenza durante a gestação não evidenciou danos para a mãe e o feto.
Estudo recente mostrou que em torno de 50% dos recém-natos não foram hospitalizados devido à Influenza em gestantes que foram vacinadas em comparação aos recém-natos, cujas mães não foram vacinadas.
A bula do Instituto Butantan recomenda a vacinação para mulheres que estão com mais de 14 semanas de gestação durante a temporada de vacinação contra Influenza. Segundo a bula, a preferência pela vacinação a partir do segundo trimestre da gravidez se deve ao fato de se evitar associação temporal com a ocorrência de abortos espontâneos, comum durante o primeiro trimestre da gravidez.
- Quem está amamentando pode tomar a vacina?
Resposta: Sim. Não existem contraindicações formais para a administração da vacina em mulheres que se encontrem amamentando.
- Pode a gestante continuar amamentando enquanto usa a medicação antiviral para Influenza?
Resposta: Sim. Não há nenhuma evidência que a medicação antiviral para tratamento da Influenza leve a efeitos adversos na gravidez e a mãe poderá continuar amamentando.
- Como a vacina é acondicionada? Precisa de equipamento especial?
Resposta: A vacina contra Influenza deverá ser conservada em temperatura entre +2°C e +8° C e ao abrigo da luz. Não deve ser colocada no congelador ou “freezer”; o congelamento é estritamente contraindicado. Nunca congelar.
- Qual a relação entre Síndrome de Guillain-Barré e a vacina da Influenza?
A síndrome de Guillain-Barré (SGB) é caracterizada por uma polineuropatia inflamatória desmielinizante aguda, que compromete, sobretudo, os nervos periféricos e leva a graus variados de fraqueza motora progressiva e ascendente, podendo atingir os membros superiores e a face.
Muitas causas podem causar SGB: dois terços das pessoas que desenvolveram a doença relatam que tiveram previamente infecções respiratórias e gastrintestinais (diarreias). Infecção com a bactéria Campylobacter jejuni é o fator de risco mais comum para GBS. Pessoas podem desenvolver SGB após ter tido Influenza ou outras infecções, tais como por CMV ou pelo vírus Epstein Barr. Em raras ocasiões, a SGB pode ocorrer após dias ou semanas após uma pessoa ser vacinada.
Diferentemente da vacina de vírus Influenza de origem suína, utilizada em 1976 e 1977, associada com elevado risco para se desenvolver a síndrome de Guillain-Barré, as vacinas preparadas, subsequentemente, a partir de outras cepas virais, não têm sido claramente associadas com aumento da frequência de SGB; se o risco existe, provavelmente é 1 caso adicional para cada 1 milhão de pessoas vacinadas.
Qualquer pessoa pode desenvolver SGB. A incidência de SGB aumenta com a idade, sobretudo em pessoas acima de 50 anos. Pessoas que desenvolveram SGB dentro de 6 semanas após a vacinação de Influenza não deve receber uma dose adicional da vacina. Em relação aos pacientes que já tiveram a SGB, é indicado esperar pelo menos 1 ano após o episódio para se administrar alguma vacina.
Entretanto, pessoas com a Síndrome de Guillain-Barré pertencem aos grupos de alto risco de complicações graves da gripe, sendo que alguns especialistas acreditam que os benefícios da imunização justificam a vacinação destes pacientes. Entretanto, deverá ser pesado o risco / benefício.
- Crianças e adultos com doenças neurológicas crônicas podem ser vacinadas contra a Influenza?
Resposta: Se você tem uma doença neurológica crônica, você faz parte do grupo de alto risco de adquirir Influenza. Se você tem qualquer das seguintes condições neurológicas descritas abaixo, você é candidato a tomar a vacina para Influenza:
Acidente Vascular Cerebral, paralisia cerebral, esclerose múltipla, doenças hereditárias e degenerativas do sistema nervoso ou muscular, dificuldades de aprendizagem, epilepsia e lesão medular.
Procure seu médico para se informar sobre a vacinação. Por exemplo, pessoa com esclerose múltipla, ao receber a vacina para Influenza, só deve receber a infusão de Lemtrada seis meses após a vacinação.
- A vacina Influenza ao ser aplicada pode levar a Síncope?
Resposta: Sim. A síncope pode ocorrer em associação com a administração de vacinas injetáveis. Por isso, após a aplicação da vacina, a pessoa deve esperar 15 minutos antes de sair da clínica de vacinação.
- Há diferenças entre Influenza e Resfriado?
Resposta: Sim. Influenza e Resfriado são doenças distintas, causadas por vírus diferentes, mas que apresentam vários sintomas em comum. A Influenza e o Resfriado são infecções respiratórias causadas por vírus. O agente etiológico da gripe é o Myxovirus influenzae, também denominado vírus Influenza. O resfriado é causado por algumas espécies de vírus: Rinovírus (principal causa dos resfriados), Adenovírus, Vírus Sincicial Respiratório, Coronavirus, Echovirus e Paramixovirus.
Os sinais e sintomas dos resfriados aparecem dois ou três dias após a exposição ao vírus. Os mais comuns são: coriza, espirros, tosse, dor de garganta, lacrimejamento, moleza, febre baixa e de curta duração. É importante se fazer o diagnóstico diferencial com o da gripe, pois é uma doença bem mais grave.
- Quais os riscos de vacina contendo Thimerosal?
Resposta: Thimerosal é um preservativo que contém mercúrio e é usado em vacinas que contêm múltiplas doses para prevenir a contaminação ao se extrair repetidamente as doses para aplicação. Não há dados que indiquem que Thimerosal usados nas vacinas tenham causado autismo ou outros problemas individuais. Segundo o FDA/ EUA, não há evidência convincente de danos causados por pequenas doses de Thimerosal como preservativo nas vacinas de Influenza, exceto um ligeiro edema e vermelhidão no local da injeção.
Um estudo analisando a vacinação com Influenza de mais de 2000 gestantes não demonstrou nenhum efeito adverso em relação ao feto associado com a vacina da Influenza.
- Qual o papel dos adjuvantes nas vacinas?
Resposta: São substâncias adicionadas à vacina com o objetivo de aumentar a resposta imune, porém seu mecanismo de ação não é completamente conhecido. Estes levam a uma resposta imune mais persistente à vacina e permite uma dose mais baixa da vacina a ser usada. Adjuvantes em uso incluem vários sais de alumínio (alum), MF59, AS04, AS03, virossomas e monofosforil lipídio A. Por exemplo, o alumínio está presente nas vacinas que previnem Hepatite A, Hepatite B, difteria, tétano, coqueluche, Haemophilus influenzae tipo B (Hib), Papillomavirus (HPV) e infecção por pneumococos.
No ano de 2015, o FDA/EUA aprovou a primeira vacina para Influenza sazonal com adjuvante (MF59) para ser usada em adultos a partir de 65 anos de idade. Dados de aproximadamente 40 ensaios clínicos demonstraram uma boa resposta imune e bom perfil de segurança.
Nenhuma vacina para Influenza disponibilizada no Brasil, ano de 2017, contém adjuvante.
- Que é vacina para Influenza com alta dose para idosos?
Os idosos são altamente beneficiados pela vacinação, uma vez que a vacina fornece elevada proteção contra as complicações associadas à gripe, frequentes nesta faixa etária, e que são responsáveis por internações e óbito. Embora a eficácia da vacina possa ser menor neste grupo do que para os adultos jovens saudáveis.
Essa vacina foi primeiramente aprovada em 2009, e contêm 4 vezes mais antígenos do que a dose regular da vacina inativada para Gripe. A dose adicional do antígeno é para aumentar a resposta imune.
Estudo publicado em 2017, comparando a eficácia da vacina da influenza, contendo mais antígenos (60 μg – alta dose de vacina versus 15 μg – dose padrão da vacina) em adultos ≥65 anos, concluiu-se que vacina de influenza com alta dose foi significativamente mais efetiva em prevenir mortes post-influenza em 2012–2013, quando subtipo de influenza A (H3N2) circulando foi mais comum, o que não ocorreu em 2013–2014 onde o subtipo de influenza A (H1N1) foi mais prevalente.
Ensaio clínico com mais de 30,000 participantes, demonstraram que os adultos com 65 anos ou mais que receberam a vacina em dose alta tiveram 24% menos de infecções por influenza, em comparação com aqueles que receberam uma vacina contra a gripe de dose padrão.
- Qual a relação entre Narcolepsia e vacina de Influenza?
Resposta: A narcolepsia é uma doença neurológica crônica que se caracteriza por uma sonolência diurna excessiva, muitas vezes incontrolável, que provoca episódios de sono súbito.
A vacina Pandemrix foi produzida na Europa pela GlaxoSmithKline e foi desenvolvida especificamente para a cepa pandêmica 2009 H1N1. A vacina Pandemrix tem na sua composição um adjuvante chamado ASO3 (esqualeno), cujo objetivo foi aumentar a resposta imune.
Cientistas do Reino Unido encontraram evidências científicas em relação à associação entre a vacina Pandemrix 2009 H1N1 e narcolepsia em crianças na Inglaterra – HPA (Health Protection Agency). Esses achados são consistentes com estudos realizados na Finlândia e outros países da Europa. No estudo finlandês e inglês foram de 0,6 a 0,9 casos a cada 100.000 doses de vacina e não se encontrou mais a associação em anos subsequentes.
Em 2014, o CDC / EUA publicou um estudo, cujo objetivo foi verificar se havia associação entre vacina pandêmica 2009 H1N1 e vacina Influenza sazonal 2010/2011 e narcolepsia. A análise incluiu mais de 650.000 pessoas que receberam a vacina Influenza pandêmica 2009 H1N1 e mais de 870.000 pessoas que receberam a vacina sazonal 2010/2011. O estudo concluiu que a vacinação não foi associada com aumento de risco para narcolepsia. Convém ressaltar que a vacina Pandemrix 2009 H1N1 com adjuvante AS03 nunca foi licenciada nos EUA. Nunca foi usado adjuvante na vacina para Influenza sazonal nos EUA.
- Qual a relação entre Síndrome Óculo-respiratória e vacina da Influenza?
Em 2000-2001, o Sistema de Saúde do Canadá, foi notificado da presença de sintomas/sinais incomuns após a imunização contra a Influenza. Estes sintomas foram posteriormente descritos como Síndrome Óculo-Respiratória.
A síndrome Óculo-respiratória ocorre dentro de 24 horas após a imunização, caracterizada por olhos hiperemiados, sintomas respiratórios, tais como tosse, sibilos, aperto no peito, dificuldade em respirar, dificuldade em engolir, rouquidão, dor de garganta e ou edema facial. Embora o mecanismo fisiopatológico permaneça desconhecido, parece ser uma resposta alérgica mediada por IgE. Esses casos são raríssimos e dentro de 24-48 horas regridem os sintomas. A depender da gravidade do quadro clínico o paciente não deverá receber posteriormente a vacina para influenza.
- O uso de medicamentos contendo estatinas altera a eficácia da vacina Influenza?
Resposta: Em dois recentes estudos foi levantada a possibilidade da estatina diminuir a eficácia da vacina em idosos. Entretanto, segundos os especialistas, necessários se fazem mais estudos sobre esse tema para se verificar a necessidade de suspensão temporária da estatina no período em a pessoa vai ser vacinada. Portanto, a vacinação é recomendada.
- Os pacientes com imunossupressão podem tomar a vacina para Influenza?
Resposta: Sim, recordando que deverá ser sempre a vacina de vírus inativado (a única disponível entre nós). Alguns pacientes com imunossupressão podem ter uma resposta imunológica baixa.
– HIV/ AIDS;
– Transplantados de órgãos sólidos e medula óssea;
– Doadores de órgãos sólidos e medula óssea cadastrados nos programas de doação;
– Imunodeficiências congênitas;
– Usuários de drogas ilícitas;
– Terapia imunossupressora, incluindo o uso ao longo prazo de corticosteroides, anticorpos monoclonais, quimioterapia, radioterapia e determinadas drogas antirreumáticas.
– Neoplasias incluindo Leucemia, linfoma de Hodgkin e não Hodgkin, Mieloma Múltiplo e outras neoplasias.
– Anemia Falciforme e outras hemoglobinopatias.
- Quais as medidas usadas para o paciente ao se dirigir ao Serviço de Saúde com sintomas de Infecção Respiratória?
– Qualquer pessoa com suspeita de Infecção Respiratória, ao chegar à emergência, deve receber uma máscara cirúrgica e ser alocado em local reservado para evitar a disseminação do vírus da Gripe.
– A pessoa, ao ser direcionada para fazer qualquer exame, deve usar a máscara cirúrgica e o setor deve ser avisado da possibilidade do paciente estar com Influenza.
- Paciente com Influenza, que requer hospitalização, quais são as recomendações?
– Precauções padrão – é aplicada para todos os pacientes, independentemente do diagnóstico ou suspeita de infecção:
- Higienização das mãos;
- Utilizar EPI (luvas, máscara, avental, protetor ocular), de acordo com o grau de exposição;
- Descarte seguro de perfurocortantes (não encapar ou desconectá-las).
– Precauções para Gotículas (Respiratórias): Indicada para pacientes com infecção transmitida por gotículas (maiores de 5µ), através de tosse, fala e espirro (ex: Influenza sazonal, rubéola, meningite, adenovírus):
- Quarto privativo ou coorte (pacientes com o mesmo microrganismo);
- Higienização das mãos;
- Usar máscara cirúrgica ao entrar no quarto privativo e retirar antes de deixar o quarto, desprezando-a no lixo e, imediatamente, fazer higienização das mãos com álcool a 70%;
- Se o paciente sob Precaução Respiratória precisar se deslocar para realizar exames ou para outra unidade do hospital deve usar uma máscara cirúrgica. Informar ao setor antes de remover o paciente;
– Isolamento no quarto privativo para crianças e adultos imunocompetentes: deverá ser mantido por 7 dias após o começo dos sintomas ou até 24 horas após a resolução da febre e sintomas respiratórios sem uso de antitérmico.
- Obs.: Crianças menores de 12 anos podem eliminar vírus por até 14 dias.
- Dentro do possível, evitar visitas ao paciente internado com Influenza. O visitante deverá usar máscara cirúrgica, evitar tocar em superfícies ou artigos e higienizar as mãos com álcool a 70% imediatamente após retirada da máscara cirúrgica.
- Qual a orientação do tempo de isolamento para pacientes adultos e crianças com imunossupressão com Influenza?
– Não existe consenso na literatura definindo o tempo ideal para esses pacientes ficar em isolamento.
– Pacientes com imunossupressão grave pode disseminar o vírus por semanas ou meses.
– Há quem recomende manter esses pacientes em isolamentos enquanto hospitalizados.
- Apesar dessas considerações acima, recomenda-se: Isolamento no quarto privativo – para crianças e adultos com imunossupressão por no mínimo 15 dias após o começo dos sintomas.
- Observações:
– O teste ideal é se realizar RT-PCR. O teste com resultado negativo, poderá ser descontinuado o isolamento mesmo antes da resolução dos sintomas respiratórios. O teste com resultado positivo indica a detecção do vírus da Influenza (RNA), confirmando a infecção. Entretanto, pode ocorrer detecção de partículas virais não infectantes, ou seja, o paciente não é contagioso.
- Quando o profissional de saúde deve usar máscara para aerossóis?
Resposta: Em procedimentos com risco de geração de aerossóis (ex: intubação, aspiração, broncoscopia, necropsia, reanimação cardiopulmonar). Realizar em quarto privativo e, se possível, em unidade de isolamento respiratório com pressão negativa e filtro HEPA.
Vigilância Sentinela de Influenza – M. Saúde – Síndrome Gripal (SG)Até a Semana Epidemiológica 52 de 2016 as unidades sentinelas de SG coletaram 20.385 amostras – é preconizada a coleta de 05 amostras semanais por unidade sentinela. Destas, 16.705 (81,9%) foram processadas e 20,7% (3.462/16.705) tiveram resultado positivo para vírus respiratórios, das quais 2.499 (72,2%) foram positivos para influenza e 964 (27,8%) para outros vírus respiratórios (VSR, Parainfluenza e Adenovírus). Dentre as amostras positivas para influenza, 1.561 (62,5%) foram decorrentes de influenza A(H1N1)pdm09, 757 (30,3%) de influenza B, 137 (5,5%) de influenza A não subtipado e 43 (1,7%) de influenza A(H3N2). Entre os outros vírus respiratórios houve predomínio da circulação 448 (46,5%) de VSR.
Da Redação do Agenda Capital










